Sisältö
- Annostus
- Suositusten määrääminen
- Yleiset haittavaikutukset
- Huumeiden vuorovaikutus
- Vasta-aiheet ja näkökohdat
Yhdysvaltain elintarvike- ja lääkevirasto (FDA) hyväksyi Harvonin 10. lokakuuta 2014 käytettäväksi yli 18-vuotiaille aikuisille, joilla on HCV-genotyypin 1 infektio, mukaan lukien kirroosi.
Harvoni on hyväksytty käytettäväksi aiemmin hoitamattomilla ("hoitamattomilla") potilailla sekä potilailla, joilla on osittainen tai ei lainkaan vastetta aikaisempaan HCV-hoitoon ("hoitokokemus").
Harvoni on ensimmäinen FDA: n hyväksymä HCV-lääke, jota ei tarvitse ottaa joko pegyloidun interferonin (peg-interferoni) tai ribaviriinin kanssa (kaksi lääkettä, joita perinteisesti käytetään HCV-yhdistelmähoitoon, molemmilla oli korkea toksisuusprofiili).
Harvonin parannusnopeuden on ilmoitettu olevan 94-99%, kun taas vaiheen II tutkimuksissa on ilmoitettu 100-prosenttinen parantumisaste potilailla, joilla on samanaikainen HIV- ja HCV-infektio.
Annostus
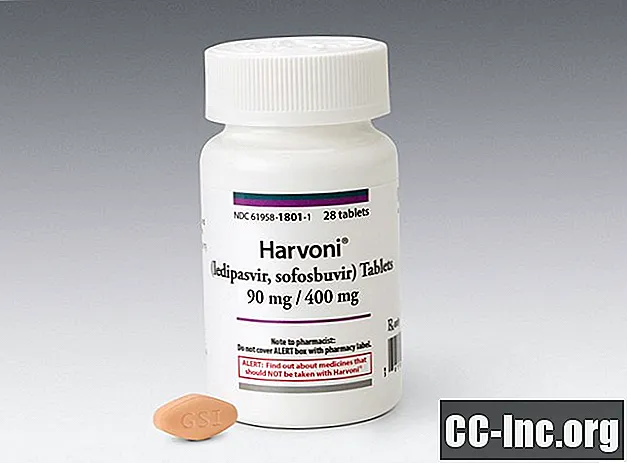
Yksi tabletti (90 mg / 400 mg) päivittäin ruoan kanssa tai ilman. Harvoni-tabletit ovat timantinmuotoisia, inkiväärinvärisiä ja kalvopäällysteisiä, joiden toiselle puolelle on kohokuvioitu "GSI" ja toiselle puolelle "7985".
Suositusten määrääminen
Harvoni määrätään 12–24 viikon kurssille seuraavien suositusten mukaisesti:
- Hoitamaton hoito maksakirroosilla tai ilman: 12 viikkoa
- Hoito kokenut ilman kirroosia: 12 viikkoa
- Kirroosilla hoidettu hoito: 24 viikkoa
Lisäksi 8 viikon hoitojaksoa voidaan harkita hoitamattomille potilaille, joilla ei ole kirroosia ja joiden HCV-viruskuormitus on alle 6 miljoonaa kopiota / ml.
Yleiset haittavaikutukset
Harvonin käyttöön liittyvät yleisimmät haittavaikutukset (esiintyy enintään 10%: lla potilaista) ovat:
- Väsymys
- Päänsärky
Muita mahdollisia haittavaikutuksia (alle 10%) ovat pahoinvointi, ripuli ja unettomuus.
Huumeiden vuorovaikutus
Harvonia käytettäessä tulisi myös välttää seuraavia:
- Rifampiinipohjaiset tuberkuloosilääkkeet: Mycobutin, Rifater, Rifamate, Rimactane, Rifadin, Priftin
- Antikonvulsantit: Tegretol, Dilantin, Trileptal, fenobarbitaali
- Aptivus (tipranaviiri / ritonaviiri), jota käytetään HIV-antiretroviruslääkityksessä
- Mäkikuisma
Vasta-aiheet ja näkökohdat
Harvonin käytölle ei ole vasta-aiheita potilailla, joilla on HCV-genotyyppi 1.
Tenofoviirilääkettä (mukaan lukien Viread, Truvada, Atripla, Complera, Stribild) käyttävillä HIV-potilailla on kuitenkin oltava erityisen varovainen mahdollisten tenofoviiriin liittyvien haittavaikutusten, erityisesti munuaisten (munuaisten) vajaatoiminnan, seurannassa.
Antasidit tulisi ottaa erikseen 4 tuntia ennen Harvoni-annosta tai sen jälkeen, kun taas protonipumpun estäjien ja H2-reseptorin estäjien (eli H2-salpaajien) annoksia voidaan joutua pienentämään ledipasviirin imeytymisen vähenemisen estämiseksi.
Vaikka Harvonin käytöstä raskauden aikana ei ole vasta-aiheita, kliinistä tietoa ihmisistä on vähän. Eläintutkimukset sekä ledipasviirin että sofosbuviirin käytöstä eivät kuitenkaan ole osoittaneet mitään vaikutusta sikiön kehitykseen. Asiantuntijoiden kuulemista suositellaan raskauden aikana Harvoni-hoidon kiireellisyyden arvioimiseksi, erityisesti siitä, aloitetaanko heti vai odotetaanko synnytyksen jälkeen.
On suositeltavaa, että kaikkia hedelmällisessä iässä olevia naisia seurataan kuukausittain hoidon aikana raskauden varalta. On myös suositeltavaa, että potilaalle ja hänen miespuoliselle kumppanilleen annetaan vähintään kaksi ei-hormonaalista ehkäisymenetelmää ja että niitä käytetään hoidon aikana ja kuuden kuukauden ajan sen jälkeen.
Hepatiitti C-lääkärin keskusteluopas
Hanki tulostettava oppaamme seuraavaa lääkärisi tapaamista varten, jotta voit kysyä oikeita kysymyksiä.

- Jaa
- Voltti
- Sähköposti
- Teksti