
Sisältö
Kaikki alla oleva sisältö on otettu kokonaisuudessaan CDC Shingles Vaccine -tietolausekkeesta (VIS): www.cdc.gov/vaccines/hcp/vis/vis-statements/shingles.html
CDC-katsaustiedot Shingles VIS: lle:
- Sivu on viimeksi tarkistettu: 12. helmikuuta 2018
- Sivu viimeksi päivitetty: 12. helmikuuta 2018
- VIS: n päivämäärä: 12. helmikuuta 2018
Sisältölähde: National Immunization Center ja Immunatory Diseases
Tiedot
Mikä on vyöruusu?
Vyöruusu (jota kutsutaan myös herpes zosteriksi tai vain zosteriksi) on kivulias ihottuma, usein rakkuloita. Vyöhykkeitä aiheuttaa varicella zoster-virus, sama virus, joka aiheuttaa vesirokkoa. Kun sinulla on vesirokko, virus pysyy kehossasi ja voi aiheuttaa vyöruusua myöhemmin elämässä.
Et voi tarttua vyöruusuun toiselta henkilöltä. Kuitenkin joku, jolla ei ole koskaan ollut vesirokkoa (tai vesirokko-rokotetta), voisi saada vesirokkoa joku, jolla on vyöruusu.
Vaipan ihottuma esiintyy yleensä kasvojen tai kehon toisella puolella ja paranee 2–4 viikon kuluessa. Sen pääasiallinen oire on kipu, joka voi olla vakava. Muita oireita voivat olla kuume, päänsärky, vilunväristykset ja vatsavaivat. Hyvin harvoin vyöruusuinfektio voi johtaa keuhkokuumeeseen, kuulo-ongelmiin, sokeuteen, aivojen tulehdukseen (enkefaliittiin) tai kuolemaan.
Noin 1 henkilölle 5: stä voimakas kipu voi jatkua kauan sen jälkeen, kun ihottuma on poistunut. Tätä pitkäkestoista kipua kutsutaan postherpeettiseksi neuralgiaksi (PHN).
Vyöruusu on paljon yleisempää 50-vuotiailla ja vanhemmilla kuin nuoremmilla ihmisillä, ja riski kasvaa iän myötä. Se on myös yleisempää ihmisillä, joiden immuunijärjestelmä on heikentynyt sairauden, kuten syövän, tai lääkkeiden, kuten steroidien tai kemoterapian, vuoksi.
Yhdysvalloissa vähintään 1 miljoona ihmistä saa vyöruusu.
Shingles-rokote (elävä)
FDA hyväksyi vuonna 2006 elävän vyöruusun rokotteen. Kliinisessä tutkimuksessa rokote vähensi vyöruusun riskiä noin 50% 60-vuotiailla ja sitä vanhemmilla. Se voi vähentää PHN: n todennäköisyyttä ja vähentää kipua joillakin ihmisillä, jotka saavat edelleen vyöruusua rokotuksen jälkeen.
Elävien vyöruusujen rokotteen suositeltu aikataulu on kerta-annos aikuiset 60 vuotta täyttäneet.
Jotkut ihmiset eivät saa saada tätä rokotetta
Kerro rokotteen tarjoajalle, jos:
Onko sinulla vakavia, hengenvaarallisia allergioita. Henkilöä, jolla on koskaan ollut hengenvaarallinen allerginen reaktio elävien vyöruusujen rokotteen annoksen jälkeen tai jolla on vakava allergia jollekin tämän rokotteen aineosalle, voidaan neuvoa olemaan rokottamatta. Kysy terveydenhuollon tarjoajalta, jos haluat tietoa rokotekomponenteista.
Olet raskaana tai epäilet olevasi raskaana. Raskaana olevien naisten tulee odottaa elävän vyöruusun rokotetta, kunnes he eivät enää ole raskaana. Naisten tulee välttää raskautta vähintään 1 kuukausi sen jälkeen, kun olet saanut vyöruusun rokotteen.
On heikentynyt immuunijärjestelmä sairauden (kuten syöpä tai AIDS) tai lääketieteellisten hoitojen (kuten säteilyn, immunoterapian, suuriannoksisten steroidien tai kemoterapian) vuoksi.
Ei tunne hyvin. Jos sinulla on lievä sairaus, kuten kylmä, voit ehkä saada rokotteen tänään. Jos olet sairastunut kohtalaisesti tai vakavasti, sinun pitäisi odottaa, kunnes olet toipunut. Lääkärisi voi neuvoa sinua.
Rokotteen reaktion riskit
Kaikilla lääkkeillä, mukaan lukien rokotteet, on reaktioiden mahdollisuus.
Elävän vyöruusun rokotuksen jälkeen henkilö voi kokea:
- Punoitusta, kipua, turvotusta tai kutinaa pistoskohdassa
- Päänsärky
Nämä tapahtumat ovat yleensä lieviä ja menevät yksin.
Harvoin elävien vyöruusujen rokote voi aiheuttaa ihottumaa tai vyöruusua.
Muita asioita, jotka voisivat tapahtua tämän rokotteen jälkeen:
- Ihmiset heikkenevät joskus lääketieteellisten toimenpiteiden jälkeen, mukaan lukien rokotus. Noin 15 minuutin istuminen tai makuuasento voi auttaa pyörtymisen aiheuttamia pyörtymistä ja vammoja. Kerro palveluntarjoajalle, jos tunnet huimausta tai jos sinulla on näköhäiriöitä tai soitat korvissa.
- Jotkut ihmiset saavat olkapään kipua, joka voi olla vakavampi ja kestävämpi kuin rutiininomainen arkuus, joka voi seurata injektioita. Tämä tapahtuu hyvin harvoin.
- Kaikki lääkkeet voivat aiheuttaa vakavan allergisen reaktion. Tällaiset reaktiot rokotteeseen arvioidaan noin 1 miljoonaksi annokseksi, ja ne tapahtuvat muutaman minuutin tai muutaman tunnin kuluttua rokotuksesta.
Kuten minkä tahansa lääkkeen tapaan, rokotteen mahdollisuus aiheuttaa vakavan vamman tai kuoleman.
Rokotteiden turvallisuutta seurataan aina. Lisätietoja on osoitteessa www.cdc.gov/vaccinesafety.
Entä jos on vakava ongelma?
Mitä minun pitäisi etsiä?
Etsi mitään, joka koskee sinua, kuten merkkejä vakavasta allergisesta reaktiosta, erittäin kuumasta tai epätavallisesta käyttäytymisestä.
Vaikean allergisen reaktion merkkejä voivat olla nokkosihottuma, kasvojen ja kurkun turvotus, hengitysvaikeudet, nopea sydämen syke, huimaus ja heikkous. Nämä alkavat yleensä muutaman minuutin - muutaman tunnin kuluttua rokotuksesta.
Mitä minun pitäisi tehdä?
Jos luulet, että kyseessä on vakava allerginen reaktio tai muu hätätila, joka ei voi odottaa, soita 9-1-1 tai lähetä sairaalaan. Muussa tapauksessa soita terveydenhuollon tarjoajaasi.
Sen jälkeen reaktio tulee ilmoittaa rokotteen haittavaikutusten raportointijärjestelmälle (VAERS). Lääkärisi tulee toimittaa tämä raportti, tai voit tehdä sen itse VAERS-sivuston kautta tai soittamalla 1-800-822-7967.
VAERS ei anna lääkärin neuvoja.
Miten voin oppia lisää?
- Kysy terveydenhuollon tarjoajalta. Hän voi antaa sinulle rokotepaketin tai ehdottaa muita tietolähteitä.
- Soita paikalliselle tai valtion terveysosastolle.
- Ota yhteyttä tautien valvontakeskuksiin (CDC) soittamalla numeroon 1-800-232-4636 (1-800-CDC-INFO) tai käymällä CDC: n rokotteiden verkkosivuilla.
kuvat
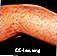
Herpes zoster (vyöruusu) käsivarteen
Herpes zoster (vyöruusu) rinnassa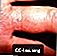
Herpes zoster (vyöruusu) kädellä ja sormilla
Herpes zoster (vyöruusu) takana
Viitteet
Sairausvalvonta- ja ehkäisymiskeskukset. Elävä zoster-rokote, ZVL. www.cdc.gov/vaccines/hcp/vis/vis-statements/shingles.html. Päivitetty 12. helmikuuta 2018. Pääsy 13. helmikuuta 2018.
Arvostelun päivämäärä 2/13/2018
Päivitetty: David Zieve, MD, MHA, lääketieteellinen johtaja, toimittajajohtaja Brenda Conaway ja A.D.A.M. Toimituksellinen tiimi. Toimituksellinen päivitys 10/30/2018.